 In de wereld van de menselijke economie, politiek, en de samenleving, er zijn veel verschillende valuta's, die allemaal worden verhandeld voor goederen. Dit kan olie zijn, Amerikaanse dollars, Facebook-likes of oma's cookies. De natuurlijke wereld heeft vergelijkbare valuta:handel in zuurstof, koolstof, en misschien wel de meest waardevolle valuta van allemaal: stikstof- .
In de wereld van de menselijke economie, politiek, en de samenleving, er zijn veel verschillende valuta's, die allemaal worden verhandeld voor goederen. Dit kan olie zijn, Amerikaanse dollars, Facebook-likes of oma's cookies. De natuurlijke wereld heeft vergelijkbare valuta:handel in zuurstof, koolstof, en misschien wel de meest waardevolle valuta van allemaal: stikstof- .
De hele wereld vecht ervoor, eerlijk oogsten, er voor vals spelen, en het op brute wijze stelen. Het is een krachtig element, in de hoogste hoeveelheden nodig voor een goede groei, verdediging, en reproductie. Dit artikel gaat over wat stikstof is, waar het voorkomt in het systeem, en hoe het samenwerkt met de andere elementen van aquaponics. Ook bespreken we hoe u een stikstoftekort kunt herkennen.
Zoals ik al zei, stikstof is een van de belangrijkste voedingsstoffen in uw aquaponic-systeem. Het komt in verschillende vormen voor in de natuurlijke wereld, maar voor nu, we zullen ons concentreren op de meest relevante:eiwit.
Eiwit is opgebouwd uit aminozuren, die zelf zijn opgebouwd uit stikstof. Alle planten en dieren bevatten eiwitten, en als ze sterven, andere organismen consumeren ze en vangen deze eiwitten op voor energie. Dus, stikstof komt het lichaam binnen in de vorm van eiwitrijk voedsel.
Wanneer landdieren eiwitten consumeren, breken ze deze uiteindelijk af tot aminozuren en vervolgens tot ammoniak. Ammoniak (NH3) is smerig spul - het is erg giftig - en de beste manier om overtollige ammoniak kwijt te raken, is door het uit te scheiden. Dus, bij landdieren, ammoniak wordt omgezet in een chemische stof genaamd ureum en uitgescheiden in de urine.
Stikstof komt op vrijwel dezelfde manier voor in aquaponic-systemen. Het komt binnen in de vorm van visvoer. De vissen consumeren het voedsel, maar het proces is eenvoudiger; de microben in hun buik breken de eiwitten af tot ammoniak en ammonium. Ammoniak is meestal aanwezig als ammonium (NH4+) dat zich door de celmembranen van de vissen beweegt en uiteindelijk in het water diffundeert. Geen extra conversie nodig. voor vissen, hoe dan ook.
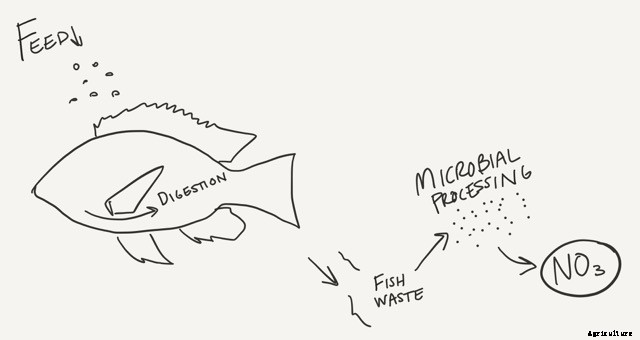
Afhankelijk van de pH van uw water, ammonium kan ammonium blijven of veranderen in ammoniak, wat erg gevaarlijk kan zijn. Ammoniak heeft geen lading, dus de vissen hebben moeite om het uit hun lichaam te houden. Wanneer dit gebeurt, de vissen zijn vergiftigd.
Dus, zodra ammoniak in de oplossing is, het moeten worden getransformeerd of het zal uiteindelijk de vis doden. Er zijn twee manieren om dit te doen:verander je pH om de voorkeur te geven aan ammonium (wat niet wordt gesuggereerd) of zet de ammoniak om in nitraten. De reeks transformaties van een organische vorm (ammoniak) naar een voor planten beschikbare vorm (nitraat) - en de volgende stap in de cyclus - heet nitrificatie.
Nitrificatie is het proces dat de meeste aquaponic-systemen aandrijft. Eigenlijk, nitrificatie zet ammoniak en ammonium om in bruikbaar nitraat. Dit gebeurt in twee processen:ammoniak omzetten in nitriet, en het omzetten van nitriet in nitraat.
In bijna alle omgevingen (behalve anaërobe omgevingen) wordt ammoniak snel omgezet in nitriet (NO2-). microben - of nitrificerende bacteriën —in de bodem of oplossing zuurstof toevoegen aan (of oxideren ) de ammoniak. Terwijl dit gebeurt, de microben krijgen de energie om koolstof te fixeren (koolstof afbreken van koolstofdioxide om cellen te bouwen). In aanvulling, waterstofionen (H+) worden geproduceerd - de ionen die worden gemeten in de pH-test en ervoor zorgen dat water zuur wordt.
Dit proces wordt traditioneel toegeschreven aan een bacterie genaamd Nitrosomonas. Recent onderzoek toont aan dat er vele honderden, zo niet duizenden verschillende soorten naast Nitrosomonas die dit werk ook doen.
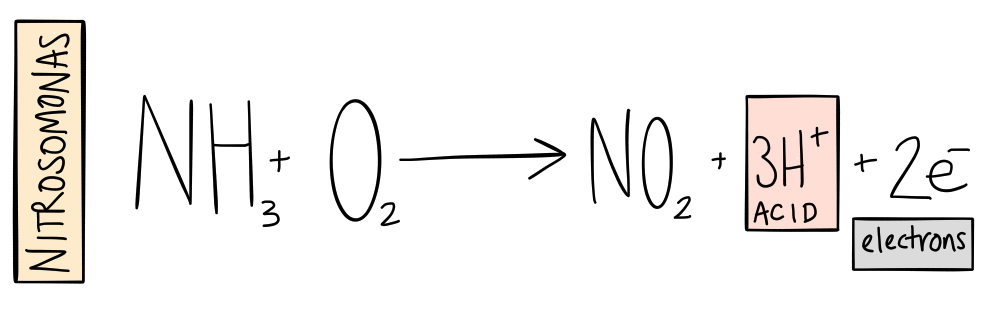
Dat is stap één.
De volgende stap in de cyclus is om dat nitriet om te zetten in nitraat. Nitriet is ook behoorlijk giftig, dus je wilt nooit teveel in je systeem. Gelukkig, het vertegenwoordigt veel opgeslagen energie voor andere [nitrificerende] bacteriën. Deze bacteriën oxideren het nitriet en gebruiken de energie van het proces om meer koolstof vast te leggen. Klinkt bekend, behalve deze keer is het resultaat nitraat (NUMMER 3-). Nitraat is een relatief niet-toxische vorm van stikstof die planten kunnen opnemen en gebruiken om cellen te bouwen.
De bacterie die het meest is erkend voor het uitvoeren van deze chemische reactie, wordt Nitrobacter genoemd. Opnieuw, echter, onderzoek wijst uit dat er naast Nitrobacter veel bacteriën zijn die aan deze reactie deelnemen.
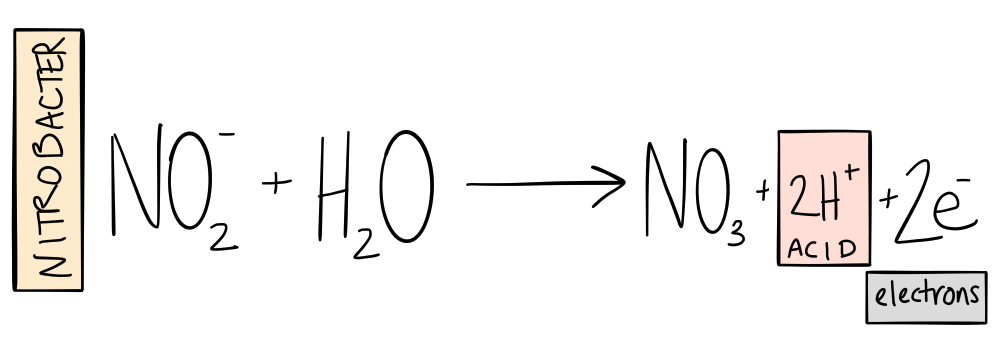
Terwijl de bacteriën ammoniak en nitriet oxideren, ze geven hydroniumionen af aan de oplossing, waardoor het systeem zuurder wordt. (Voor mensen die hun systemen in het optimale pH-bereik willen laten werken voor de beschikbaarheid van voedingsstoffen, nitrificatie is het belangrijkste proces voor het verlagen van de pH). Dit geeft aan waarom de oplossing van oudere systemen naar meer zure pH-waarden neigt.
Stikstof is beschikbaar met een groot aantal pH-waarden, dus pH is minder belangrijk als het gaat om de beschikbaarheid van stikstof.
"... nitrificatie is het allerbelangrijkste proces voor het verlagen van de pH."
De snelheid waarmee de pH van een oplossing verandert, echter, kan de beschikbare vorm van stikstof beïnvloeden (zie de video over ammoniak/ammonium en pH) evenals de efficiëntie van nitrificatie. Als nitrificerende bacteriën geen tijd krijgen om zich aan te passen aan veranderende pH-waarden (zoals bijna elke andere systeemvariabele), nitrificatie zal lijden.
In feite, nitrificatie verloopt prima bij lage pH-waarden, zolang de nitrificerende ecologie de tijd krijgt om zich aan te passen. Nitrificerende bacteriën zijn over het algemeen inefficiënt als het gaat om het wijzigen van systeemvariabelen. Ze sterven vaak af of gaan slapen wanneer ze worden blootgesteld aan te veel licht, temperatuurschommelingen, fluctuaties in zoutgehalte en pH, evenals vele andere veranderingen in hun omgeving.
De waargenomen balans tussen pH en nitrificatie-efficiëntie is gebaseerd op de veronderstelling dat nitrificatieactiviteit in aquaponic-systemen voornamelijk een functie was van twee verschillende groepen bacteriën: Nitrosomonas spp., en Nitrobacter spp.
In laboratoriumproeven, deze bacteriesoorten zijn gevoelig gebleken voor pH, met veranderingen in pH die hun vermogen om ammoniak (Nitrosomonas) en nitriet (Nitrobacter) te oxideren, beïnvloeden. Onthoud dat de meeste nitrificerende bacteriën (in ieder geval tot nu toe bestudeerd) niet goed omgaan met veranderende omgevingsvariabelen. Dit is om twee redenen belangrijk om te weten:
Wat heeft dit te maken met het nitrificatiedebat? We zullen, Punt 1 vertelt ons dat misschien veel van de "systeemcrashes" die worden toegeschreven aan een te lage systeem-pH, in feite kunnen worden toegeschreven aan het te snel verlagen van de systeem-pH. Punt #2 vertelt ons dat Nitrosomonas en Nitrobacter misschien niet echt de meest belangrijke nitrifiers in systemen - het zijn gewoon de gemakkelijkste groepen om te isoleren en te laten groeien in een petrischaal in een laboratorium.
Het betekent in feite dat de harde en snelle regels van nitrificatie misschien niet zo hard en snel zijn als ze doorgaans worden gecommuniceerd. Er zijn veel systemen met zeer lage pH-bereiken met een hoge nitrificatie-efficiëntie (inclusief de onze). Het kan zijn dat Nitrosomonas en Nitrobacter-soorten de primaire nitrificeerders in ons systeem zijn, maar de realiteit is dat we het gewoon niet weten. Wat we wel weten, is dat onze nitrificatie efficiënt en uitstekend is, ongeacht de pH van ons systeem.
Om dit in perspectief te plaatsen, er zijn veel zure bodems en mariene milieus over de hele wereld waar nitrificatie plaatsvindt bij opmerkelijk lage pH-bereiken. Veel van de nitrificeerders in deze omgevingen zijn geen lid van de Nitrobacter- of Nitrosomonas-groepen. Velen van hen zijn onbekend. In een enkele schep aarde, er zijn er naar schatting 10, 000 verschillende soorten bacteriën of ongeveer het dubbele van het aantal bacteriën dat de wetenschap momenteel kent.
Met dat in gedachten, Ik denk dat het niet zomaar kan, maar waarschijnlijk zijn er enkele behoorlijk interessante bacteriën die nitrificerende functies vervullen in aquaponic-systemen over de hele wereld.
Bekijk onze BSA-video met details over het biologische oppervlak, misschien wel het belangrijkste systeemontwerpelement dat nitrificatie bevordert.
 In elk geval, het eindproduct is nitraat (NO3-). Sommige planten kunnen ammonium opnemen en gebruiken. Echter, de meeste voorkeur aan nitraat. In systemen met een overmaat aan ammonium, de planten kunnen de neiging hebben om langbeniger te zijn en zijn vaak minder verkoopbaar. Anderzijds, in systemen met veel nitraten, de problemen met bladluizen en ander ongedierte kunnen dramatischer zijn, meer ingrijpen nodig. Houd er dus rekening mee dat systemen met te veel nitraten meer problemen met ongedierte kunnen zien.
In elk geval, het eindproduct is nitraat (NO3-). Sommige planten kunnen ammonium opnemen en gebruiken. Echter, de meeste voorkeur aan nitraat. In systemen met een overmaat aan ammonium, de planten kunnen de neiging hebben om langbeniger te zijn en zijn vaak minder verkoopbaar. Anderzijds, in systemen met veel nitraten, de problemen met bladluizen en ander ongedierte kunnen dramatischer zijn, meer ingrijpen nodig. Houd er dus rekening mee dat systemen met te veel nitraten meer problemen met ongedierte kunnen zien.
Nitraat, nitriet, en ammoniakniveaus kunnen eenvoudig worden getest met een zoetwatertestkit, zoals deze. Nitraat lost op in de oplossing en wordt onmiddellijk beconcurreerd door bacteriën, schimmels, algen en andere planten. Al deze organismen nemen nitraat op en gebruiken het in hun weefsels. Als de bacteriën, schimmels, en algen sterven, dat stikstof (vaak in de vorm van eiwit) opnieuw in het systeem komt en de cyclus opnieuw begint. Een groot deel van het nitraat, echter, is geleverd, veilig en wel, naar de wortelzone, waar de planten in uw systeem het opnemen en gebruiken om te groeien.
Hoewel het gevaarlijk is om ammoniak- of nitrietniveaus te hebben die veel hoger zijn dan respectievelijk 2 ppm en 1 ppm, nitraat kan vaak ver boven de 100 ppm uitkomen (ver buiten de grafiek voor veel nitraattests) zonder een bedreiging voor uw vissen te vormen. Veel hydrocultuursystemen gebruiken nitraat in het bereik van 160 ppm. Planten kunnen niveaus vaak zelfs hoger waarderen, maar de aquaponic-kweker moet een evenwicht vinden tussen de behoeften van de vissen, de systeemecologie (inclusief plagen), en de behoeften van de planten. Om deze reden, Ik raad de meeste aquaponic-kwekers aan om te schieten om hun nitraat binnen het bereik van te houden 40-80 p.p.m. voor goed, constante plantengroei.
Veel systemen hebben moeite om het stikstofgehalte op peil te houden, vooral naarmate het systeem volwassener wordt, planten worden groot en de systeemecologie wordt complexer. Dit kan betekenen dat de voeding moet worden verhoogd om aan de toegenomen vraag te voldoen. Veel mensen willen in eerste instantie de bezettingsdichtheid verhogen, maar dat is vaak een vergissing. In plaats daarvan, voersnelheden verhogen (maar niet te veel voeren!), en kijken of met dezelfde hoeveelheid vis hogere nitraatgehaltes kunnen worden bereikt.

Aangezien stikstof een mobiele voedingsstof is (het wordt naar verschillende plaatsen in de plant geleid), tekortkomingen beïnvloeden eerst de oudere groei. Symptomen van een tekort zijn totale chlorose zonder patroon op het blad en groeiachterstand. Lees onze beginnershandleiding voor voedingstekorten voor meer informatie.
Naast visvoer, stikstof komt het systeem binnen via meststoffen. Bijna alle meststoffen hebben een NPK-classificatie die u de relatieve concentraties stikstof aangeeft, fosfor, en kalium (in die volgorde). Voor vegetatieve groei (de groei van stengels, bladeren, en wortels), stikstof is meer nodig dan welke andere minerale voedingsstof dan ook.
Op veel manieren, stikstof is de belangrijkste voedingsstof voor planten, maar ook de eenvoudigste. De volgende voedingsstof op onze lijst is ijzer - een kieskeurige voedingsstof maar een belangrijke.